彭吉润医生的科普号
- 精选 晚期胰腺癌治疗也有招儿 ——微创消融治疗为“老王们”带来了福音
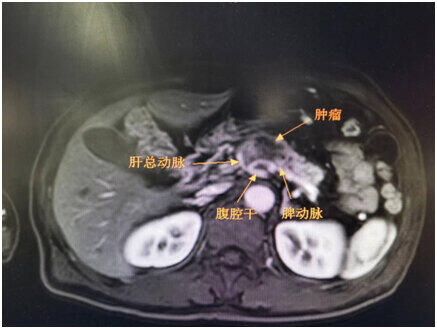
“肚子怎么又不舒服了呢,难不成吃了坏东西了?”几个月前,老王心里直犯嘀咕,寻思可能是胃肠道的炎症,吃点药可能就没事了吧。可是情况越来越不对劲,腹部正中偏上那个位置的疼痛越来越明显,吃了多种胃药也不管用。短短一个月时间,熟人见了都问他,怎么瘦得快要脱相了,这才想起来去医院看看。老王和他老伴已经想不起来是怎么走出医院的了,老伴仿佛魂不附体似地冒了句:“好端端一个人,平时既不抽烟也不喝酒,怎么就得了胰腺癌,还是晚期了呢?”说完,不知不觉已泪流满面,老王是那么勤劳能干的一个人,平时也很注意保养身体,这刚退休没几年,还没来得及享福呀!回到家跟闺女说了这个坏消息,沉重的氛围一下子笼罩了整个家庭。还是闺女打破了沉默,赶紧去省城、北京的大医院瞧瞧吧。老王一家先后去了省里、北京的几家三甲医院,结论是一样的,胰腺癌侵犯了肝总动脉和肠系膜上动脉,已经没法做手术了。怀着一线希望,老王一家经朋友介绍,来到了首都医科大学附属北京世纪坛医院肝胆肿瘤外科。在诊室外等候时,全家人的心情很复杂,也很无奈,因为他们也知道,大夫看了片子后大概率会说什么样的话。轮到他们就诊时,彭吉润主任详细了解病情以后,站起身仔细看了老王的磁共振扫描片子,随后耐心地讲解道:“肿瘤位于胰腺体部靠近胰颈的部位,侵犯了重要血管(图1),传统意义上的手术是没法做了,但是可以通过手术探查,做微波消融治疗,这种方法还是一种相对微创的治疗办法,结合术后辅助治疗,也能取得比较好的效果。”图1.患者胰腺肿瘤的解剖位置关系,可见肿瘤侵犯了腹部多支重要血管胰腺癌号称癌中之王,发病率逐年上升。手术切除是胰腺癌患者获得治愈和长期生存的有效办法。但是胰腺癌患者获得诊断时,超过80%的患者往往已到晚期,肿瘤侵犯了周围组织和器官,还有的已经发生了远处转移,因此失去了手术机会。即使一部分患者能够获得手术切除,但由于胰腺的解剖位置特殊,加上胰腺癌容易发生周围组织侵犯、扩散、转移等生物学行为,手术治疗的效果也是相当有限。对于这些失去手术机会的胰腺癌患者怎么治疗呢?虽然医疗技术一直在进步,但是对这类患者的治疗还是举步维艰,收效甚微。目前可用于治疗胰腺癌的化疗药物屈指可数,疗效有限不说,副作用也比较大。虽然靶向药物及免疫疗法已经在多种肿瘤中取得了长足的进步,但是在胰腺癌中仍然进展缓慢。在这种情况下,微波消融的应用为晚期胰腺癌的治疗带来了机遇和进步。消融手术是指在B超或CT引导下,通过注射无水酒精或者通过加热、冷冻的方法使得肿瘤细胞发生坏死,达到原位灭活;通过消融治疗不但能最大程度地杀灭肿瘤细胞,还能最大限度地保护周围的正常组织结构。其中,微波消融是采用与微波炉类似的原理,首先在超声引导下将消融针直接穿刺到胰腺癌病灶中,然后通过发射微波,带动肿瘤组织中的水分子往复运动、碰撞大量产热,从而使病灶中的肿瘤细胞发生凝固性坏死。微波消融还能同时灭活侵犯腹膜后神经丛的肿瘤细胞,因此能明显缓解患者的疼痛症状。此外,灭活的肿瘤组织还能产生大量热休克蛋白,同时释放肿瘤抗原,因此可以激活人体的免疫系统,通过免疫机制杀伤残留的零星肿瘤细胞。了解到这些以后,老王和家人暗淡的眼神一下子亮了许多,多日来积压在心头的阴霾也一扫而空,当即决定入院治疗。入院后,主管医生对老王的胰腺肿瘤和全身情况进行了精准评估。经过缜密的术前准备,2022年5月27号,在麻醉科、手术室等兄弟科室的保驾护航下,彭吉润教授主刀,成功完成了超声引导下胰腺癌的微波消融治疗。手术探查发现,肿瘤主要位于胰体部,约4.5×3.0厘米大小,尽管个头不算太大,但面目狰狞,形态极不规则,侵犯了肝总动脉、门静脉前内侧壁、脾静脉、肠系膜上动脉等重要血管,以及腹后壁的软组织和横结肠系膜根部,确实没有做根治性手术切除的指证。我们首先做了穿刺活检以明确组织病理学诊断,然后在超声引导下制定了合适的穿刺路径,对胰腺肿物进行微波消融,消融范围还覆盖了超过5mm的癌旁组织,并做了周围淋巴结清扫,达到了彻底杀灭肿瘤的目的。手术过程非常顺利,手术后肿瘤标记物CA199显著下降,复查磁共振扫描,显示患者的胰腺病灶已完全失去活性(图2)。术后老王很快就顺利出院了。出院那天,风和日丽,老王特地带着家人来感谢彭吉润教授团队又给了他一次重生的机会。这是北京世纪坛医院肝胆肿瘤外科成功应用微波消融技术治疗晚期胰腺癌的又一个典型病例。彭吉润教授带领整个团队,不断进行技术创新,通过微创消融治疗,使许多像老王一样的晚期胰腺癌患者获得了很好的治疗效果,不但显著延长了生存期,并且也有很高的生活质量。在此,特别提醒大家,五十岁以上的中老年人,特别是其直系亲属中有胰腺癌患者的人,假如近期出现了以下情况,如上腹部正中的隐痛不适并且迁延不愈,短期内不明原因出现消瘦乏力,突然发现血糖轻度升高或糖耐量异常,或者全身多处出现不明原因的静脉炎症,称之为游走性血栓性静脉炎,请及时到医院就诊,排除胰腺肿瘤找上门来。图2.老王的胰腺肿瘤消融治疗后,病灶完全坏死,失去活性
 彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)427人已读
彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)427人已读 - 典型病例 冷冻消融显神威 北京世纪坛医院完成首例晚期巨大肝癌冷冻消融治疗
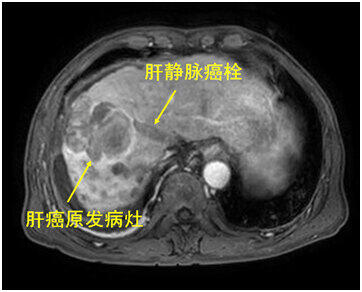
近期,首都医科大学附属北京世纪坛医院肝胆肿瘤外科首次成功地完成了一例晚期巨大肝癌的冷冻消融治疗,进一步丰富了肝癌治疗手段,使我院医院的肝脏恶性肿瘤综合治疗水平上了一个新台阶。黑龙江的周先生5个月前因右上腹部胀痛不适,行腹部B超检查,发现肝内有多个肿瘤,同时还伴有门静脉主干及分支癌栓形成,当地医院考虑是晚期肝癌,建议到上级医院治疗。于是,周先生来到北京世纪坛医院,找到了肝胆肿瘤外科主任彭吉润教授。彭教授和同事详细询问了患者病史,仔细阅读了患者的影像学等辅助检查资料,考虑患者诊断很明确,但是由于肿瘤多发,并且合并大血管如门静脉以及肝静脉内的癌栓,肿瘤还转移到了左侧肾上腺,因此不能做根治性手术切除了(图1)。图1.右肝巨块型肝癌伴门静脉和肝静脉癌栓目前肝癌已进入综合治疗时代,包括消融治疗、靶向药物治疗、免疫治疗在内的各种新疗法层出不穷,日新月异,使许多以往被迫放弃治疗的晚期肝癌患者,也能获得良好的治疗效果。针对周先生的疾病,彭吉润教授团队为其制定了局部病灶治疗加全身药物治疗相结合的个体化治疗方案:首先在超声引导下进行肝肿物活检,明确其病理学诊断。然后采用“肝动脉化疗栓塞+靶向药物+免疫治疗”的方案进行综合治疗。在此基础上,为了进一步增强前期的治疗效果,再对肝内的巨大肿瘤行冷冻消融治疗。2022年7月13日,在完成前期治疗后,经过周密术前准备,在麻醉科和手术室的精心配合下,彭吉润教授和团队成员成功地完成了这例晚期大肝癌患者的冷冻消融手术。术中,彭吉润教授和团队成员根据患者肿瘤巨大、多发的病灶特点,结合实时超声扫查结果,制定了多针穿刺和多点布针的方案。在超声科医生的协助下,彭主任使用我院新引进的康博刀,运用液氮冷冻技术,对患者的肝内肿瘤病灶尽可能适形、全面地进行了消融治疗。术后,周先生的病情得到了显著缓解,右上腹的胀痛症状消失了,术后复查磁共振扫描,证实肝脏的绝大部分病灶都已灭活(图2);行PET-CT检查显示肝静脉和门静脉内的癌栓竟然也失去了活性;而且,病人的血清肿瘤标志物甲胎球蛋白(AFP)也从5500ng/ml骤降到了13ng/ml。目前,周先生一般状况良好,仍在按照彭教授团队制定的治疗计划,按期用药,并接受定期随访。图2.冷冻消融联合介入治疗、靶向药物和免疫治疗后的效果上述病例中,肝胆肿瘤外科团队所使用是北京世纪坛医院新引进的多模态冷热消融治疗设备——康博刀,这是一种具有国际原创性知识产权、由我市科技企业生产的自主创新类医疗设备(图3)。手术中,医生首先在B超等影像设备引导下,将消融针穿刺到肿瘤中。治疗程序开启后,仪器便将液氮经内部的精密管路泵入消融针杆,使针尖部位的温度急剧降低到-196℃,从而在消融针周围形成一个4.5×4.5×5.5厘米的椭圆形超低温冰球,将肿瘤组织包裹,从而冻死肿瘤细胞以及肿瘤内的微血管。之后,该设备会通过另一个并行的密闭管路将加热的无水乙醇注入消融针杆中,使超低温冷冻组织迅速升温至80℃,从而彻底破坏肿瘤;针杆加热还能起到防止穿刺针道出血,以及防止肿瘤经穿刺针道种植转移的作用。此外,经历“冰与火”之间将近300度巨大温差,被二重杀伤的肿瘤细胞崩解后,还能释放大量的肿瘤抗原,形成原位肿瘤疫苗,诱导特异性抗肿瘤免疫应答,联合使用PD-1单抗等免疫检查点抑制剂后,可对局部残留肿瘤细胞以及远隔部位的转移性肿瘤病灶起到持久的杀伤作用。北京世纪坛医院开展的复合式液氮实体肿瘤消融治疗,不但有助于首都创新医疗器械的高质量发展和临床推广工作,也给广大肝癌患者带来新生的希望。图4康博刀及其形成的深低温冰球
 彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)873人已读
彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)873人已读 - 精选 乳腺癌合并肝转移同时行手术切除+微波消融
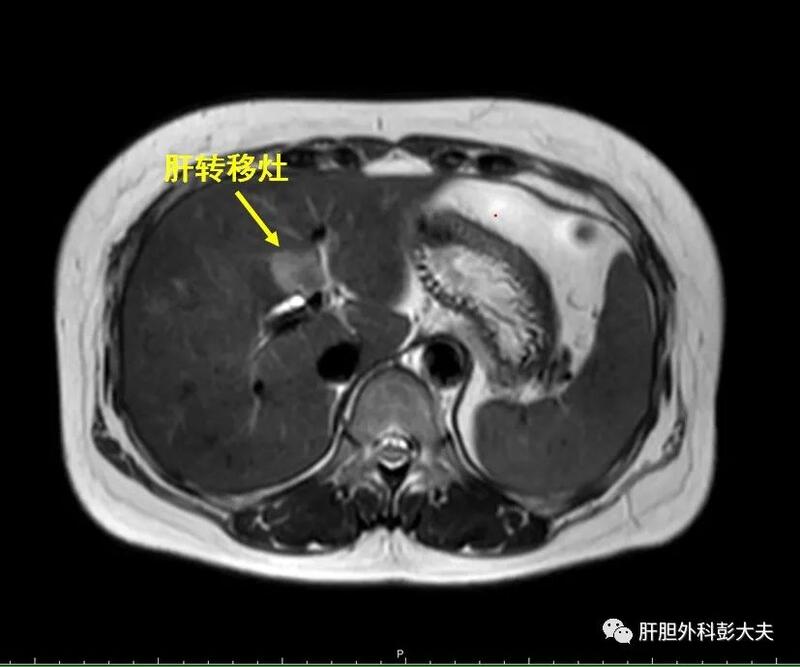
家住辽宁大连的李女士无意中发现乳腺长了一个肿物,由于并没有什么不适症状,她大约4个月后才去医院就诊。行磁共振扫描发现其右侧乳房有一个直径2cm左右、可疑恶变的结节,穿刺活检见大量癌细胞,不除外乳腺导管内癌可能。同时经上腹部磁共振扫描发现,在其肝脏左内叶也有一个直径2.2cm的转移灶。因为病情比较晚,李女士的家人带她看了多家医院,专家们给出的治疗方案都不太一致,因此一家人很纠结。来到首都医科大学附属北京世纪坛医院就诊后,再次复查乳腺磁共振扫描,提示右侧乳腺肿物大小为1.9×1.1cm,上腹部磁共振扫描及PET/CT进一步证实肝左内叶有一1.8×2.4cm的转移灶(图一)。2023-03-30行超声引导下乳腺穿刺活检术,病理诊断为:(右乳肿物)乳腺浸润性导管癌,组织学分级Ⅱ级;免疫组化示:ER(90%,+++),PR(50%,+++),HER2(2+),但复检FISH提示HER2(-)。我们和乳腺外科组织相关专家对该病例进行了MDT讨论,根据上述全面评估结果,乳腺外科的李艳萍主任建议先行新辅助化疗以达到缩小肿瘤的目的,后续再行联合手术根治肿瘤。征得李女士一家同意后,她被收入乳腺外科,自2023-04-18起,连续做了6个周期的化疗:TE方案(紫杉醇脂质体240mg+表柔比星120mg)。化疗完成后,我们再次对该患者进行了影像学检查,发现其右乳腺肿物已经缩小至14.2mm×7.8mm,而肝脏左内叶转移灶也缩小到了1.2×0.9cm(图二)。2023年9月7日,我们科室联合乳腺外科为李女士同时做了乳腺癌改良根治术+腹腔镜肝脏转移灶微波消融术。全麻成功后,我们科室首先在腹腔镜直视以及腔镜专用B超的辅助导引下,将微波消融针插入位于左肝内叶、临近门静脉左支及矢状部的转移肿瘤,对其进行了精准的微波消融治疗。之后,由乳腺外科李艳萍主任团队继续完成了乳腺部分的相关手术。整个手术过程十分顺利。手术后第2天复查上腹部磁共振扫描,显示肝脏转移瘤病灶被完全灭活(图三)。而切除的乳腺标本经术后病理检查再次证实了乳腺浸润性导管癌的诊断,且清扫的相关淋巴结中未见肿瘤转移。尽管李女士同时接受了两个器官的手术,但由于总体创伤不大,因此在医护人员的精心护理下,李女士很快就出院了。乳腺癌合并肝转移,尽管从病理分期上属于晚期,但这例病例表明,经过多学科协作,采取恰当的治疗方案,仍然能达到根治性治疗效果。
 彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)29人已读
彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)29人已读 - 精选 肝癌免疫微环境研究取得重大突破 为攻克肝癌发现新思路
光明日报北京10月31日电 记者詹媛31日从首都医科大学附属北京世纪坛医院彭吉润课题组了解到,有关肝癌免疫微环境的研究取得重大突破——在国际上首次系统分析和比较肝癌组织、癌旁正常组织、肝脏周围淋巴结、腹水和血液中免疫细胞的组成、功能状态、发育轨迹,及免疫细胞之间的相互作用。肝癌是世界上死亡率排名第三的癌症,我国的肝癌发病率居世界之首。作为在国际上具有开创性的工作,这项成果可为研究肝癌和其他癌症的免疫逃逸机制,开发更先进的临床检测与免疫治疗方案提供新的思路,对探索攻克肝癌的手段有很大潜在价值。该研究由北京大学生命科学学院、北京未来基因诊断高精尖创新中心、生物医学前沿创新中心张泽民课题组以及勃林格殷格翰公司研究人员与彭吉润课题组共同开展。据彭吉润介绍,从肝癌组织、癌旁正常组织、肝脏周围淋巴结、血液和腹水中精准收集病理标本,是这项研究顺利完成的先决条件。此次也是我国首次精准获取肝癌患者多个部位病理标本,并对其中免疫细胞进行大规模单细胞测序研究。在该项研究中,研究人员创新性地同时使用两种生物基因测序技术开展研究。他们在肝癌组织中,发现了一种高表达LAMP3分子的新型树突状的细胞,在免疫微环境中表现活跃,可以从肿瘤迁移到肝脏周围的淋巴结,并能改变人体内可“杀死”异常细胞的T淋巴细胞的状态,而且无论在人体内还是人体外,这种细胞均可被激活并生长成熟。这一发现为基于该细胞的肝癌细胞疗法提供了新思路,未来或可通过调节免疫微环境进行肿瘤治疗。同时,研究者还发现,肝癌中原本可“吞噬”细胞环境中异物的巨噬细胞亚群,表现出不同的转录状态并能从肿瘤向腹水转移。研究者发现肝癌导致的腹水中,包含巨噬细胞在内的髓系细胞和淋巴细胞分别来源于肿瘤和血液,但淋巴细胞中具有增殖活性、能杀伤肿瘤的T淋巴细胞亚群则来自肿瘤。该结果为利用肝癌病人的腹水代替外周血或活检组织进行肿瘤状态检测提供了新的思路。据了解,这项研究即将在国际顶尖科学杂志《细胞》上发表。鉴于该研究成果对人类攻克肝癌的重大意义,《细胞》杂志还将于美国东部时间31日11时(北京时间31日23时),在其官方网站面向全球在线发布这项成果。这也是张泽民和彭吉润课题组第二次将肝癌免疫研究的联合研究成果发表在这本国际著名的科学期刊上。
彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)1456人已读 - 精选 彭吉润教授与北大学者合作解析外周血游离DNA组织来源
首都医科大学附属北京世纪坛医院肝胆外科彭吉润教授与北京大学生物医学前沿创新中心(BIOPIC)、北京未来基因诊断高精尖创新中心文路副研究员合作,利用团队之前开发的甲基化CpG短串联扩增与测序技术(MCTA-Seq),探究了正常人、肝脏疾病患者与急性胰腺炎患者外周血游离DNA的组织来源。研究成果以“Comprehensive DNA methylation analysis of tissue-of-origin of plasma cell-free DNA by methylated CpG tandem amplification and sequencing (MCTA-Seq)” 为题在线发表于6月25日的《临床表观遗传学》( Clinical Epigenetics )。近年来,外周血游离DNA因其在无创产前DNA检测与肿瘤液体活检的临床应用而受到广泛关注。正常人外周血中也有一定浓度的游离DNA,主要来源于白细胞,但有多大比例来自其它组织器官尚不完全清楚。在多种疾病状态下,游离DNA浓度会显著增高,是否来自于受损组织或者另有其它来源,也是一个尚未解决的问题。DNA甲基化是DNA的主要表观遗传修饰,由于不同组织器官具有截然不同的DNA甲基化修饰模式,它非常适合于鉴别游离DNA的组织来源。在之前的研究中,课题组研发了一种分析外周血游离DNA甲基化组的新技术MCTA-Seq,在本项研究中,合作团队将该技术应用于探究外周血游离DNA在生理与病理状态下的组织来源问题。研究发现,正常人外周血游离DNA除了白细胞作为主要来源外,肝脏是另一个重要来源,正常人血浆游离DNA中肝脏来源比例为1.3%左右,提示肝脏细胞存在生理性凋亡和自我更新。对肝胆胰疾病患者血浆游离DNA进行分析后,发现肝内胆管结石患者与肝癌患者外周血中有大量肝脏DNA释放,提示肝脏细胞在这些病理状态下发生显著坏死;急性胰腺炎患者外周血中升高的游离DNA过去普遍认为可能来自受损的胰腺组织,然而,研究者通过组织来源定量分析意外发现,白细胞才是急性胰腺炎患者外周血中游离DNA升高的主要来源,推测可能与免疫系统的急性炎症激活有关;肝硬化患者的游离DNA浓度也显著高于正常人,升高的游离DNA也主要来自白细胞,这可能是脾功能亢进破坏血细胞的结果。此外,研究者还发现了一类新颖的适用于游离DNA检测的组织特异性甲基化CpG岛,这类CpG岛位于组织特异性高表达基因的内部,具有很强的组织特异性超甲基化模式。北京大学生物医学前沿创新中心、北京未来基因诊断高精尖创新中心、生命科学学院博士生刘晓萌、任杰,北京世纪坛医院肝胆外科博士生罗楠为该论文并列第一作者。文路副研究员与彭吉润教授为该论文的共同通讯作者。该研究项目得到了国家自然科学基金面上项目、北京未来基因诊断高精尖创新中心的基金支持。原文标题:Comprehensive DNA methylation analysis of tissue-of-origin of plasma cell-free DNA by methylated CpG tandem amplification and sequencing (MCTA-Seq)https://rdcu.be/bHFH3
彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)1186人已读 - 典型病例 罕见血型患者巨大肝尾状叶肿瘤被成功切除
“巨大肝尾状叶肿瘤!”4年半前,当父亲的CT报告出现在自己眼前时,小孙(化名)这个东北汉子一下子懵了。根据当地医生的描述,父亲的肿瘤长在了肝脏的尾状叶上,这个位置的肿瘤很少见,而且肝尾状叶长在一个特殊的位置,前面是供应肝脏血液的门静脉、肝动脉以及出肝的左右肝管,后面紧贴人体最大的静脉下腔静脉,上方则紧邻引流出肝血流的几条肝静脉及其汇入下腔静脉的位置,因此肝尾状叶肿瘤切除的难度和风险极大。小孙的父亲因为肿瘤很大,直径在5cm以上,并且很可能已经侵犯到了下腔静脉,手术中稍有不慎,就有可能损伤到大血管而引起致命的大出血。医生建议,“咱们这儿治不了这病,你们去北京吧。” 小孙带着父亲来到了北京,几经辗转,托熟人找到了首都医科大学附属北京世纪坛医院普外一科的彭吉润教授。彭吉润教授是我国知名的肝胆外科专家,从事肝脏外科诊疗及研究工作近30年,有着极为丰富的肝脏切除手术的经验。彭教授详细询问了病史,仔细审阅了患者的影像等辅助检查资料,考虑患者诊断明确,虽然尾状叶肿瘤较大,与下腔静脉关系密切,但经过努力,还是有切除的可能性,便将患者收治入院。 病人入院后,在术前检查及准备的过程中,又遇到一个意外的情况:血型检测显示该患者为Rh阴性血型。这是一种是非常罕见的血型,在中国表现为这种血型的人只占人群总数的0.34%,老百姓形象地将其称呼为“熊猫血型”。Rh阴性血型的人一般只能输注Rh阴性的血液,因为在其体可能会存在Rh抗体,如果输入Rh阳性的血液,将会诱发严重的急性溶血性输血反应。因为人群中Rh阴性血型的人所占比例很低,血库中这种血的库存也很少,所以很难为这种血型的患者配到足够的手术用血。肝脏手术的最大风险之一就是术中出血,更何况彭吉润教授团队所面对的是一位手术难度本身就很大的肝尾叶肿瘤患者,如果术中大量出血而无足够的备血可用,病人将处于十分危险的境地。更令人沮丧的是,时值岁末年初,正是北京市手术配血最困难的“血荒”时期,别说遇到这种罕见血型了,就是为常规血型的手术患者配血都是令北京各大医院血库主任头疼的事情。在这种情况下,如何为这名患有特殊疾病又是特殊血型的患者准备较为充足的血液成为摆在彭吉润教授团队面前的一大难题。 在彭教授的协调下,普通外科、输血科和麻醉科积极配合,采取了“三管齐下”的找血策略:术前一周,输血科首先抽取了患者自体血400ml冻存;同时,谈春荣主任和同事们积极和北京市血液中心联系,几经争取,备好了1000ml异体血;麻醉科赵斌江主任则根据病人的具体情况,决定在手术当天、手术开始前再留取患者自体血400ml。1800ml,这就是全部的备血量了,看似不少,但对一例有巨大出血风险的肝脏尾状叶肿瘤切除手术来说,压力仍然非常之大。经过和放射科专家一起反复阅读相关影像资料和充分论证,彭教授和他的外科团队制定了周密的无血切肝手术计划。 经过精心准备,患者被推进了手术室。麻醉科赵主任亲自麻醉,护士长巡台,所有辅助人员都严阵以待。一切都按照术前计划顺利进行:开腹、游离、探查,巨大的肿瘤呈现在术者眼前,跟术前的评估一致,它位于门静脉和下腔静脉之间,直径在5cm以上,位置很深,并且血运十分丰富,手术难度显然非常大。彭教授在助手的配合下,分开所有的附着韧带,充分游离肝脏,将肝后下腔静脉全程显露,并做好应急处置准备。手术难度最大的部分,是要将肿瘤与下腔静脉彻底分离,这是肝脏手术中最精细的操作,共有10余条管壁纤细、大小不一的肝短静脉将肝脏后方、肝尾叶肿瘤和下腔静脉连接在一起。彭教授用精细的动作将它们逐一分离、钳夹、切断、缝扎......直到把肿瘤与下腔静脉完全分开。切除肿瘤的时刻来到了,在切断肿瘤与正常肝脏的连接部分时,为了最大限度地保护患者的肝脏功能,彭教授决定不阻断肝门部的入肝血流,而是采用先进的电外科工作站技术对肝脏进行分离并结合精细结扎血管、胆管的办法,边切除边止血,将患者出血量降到最低,直到将肿瘤完整切除,而此时总的手术出血量仅仅200多毫升。 术后,经过普外一科医护人员的精心护理,该患者很快便康复出院,如今已经存活四年半了。在总结这名特殊患者的诊治经验及疗效时,有专家表示,肝脏尾状叶肿瘤的无血切除是肝脏外科领域的重大技术难题,这个病例的诊疗成功,表明北京世纪坛医院在肝脏外科疾病的手术治疗方面已经上了一个新的台阶。
彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)1160人已读 - 典型病例 门静脉主干长癌栓的晚期肝癌还能治吗?
在我国,肝癌是发病率较高的恶性肿瘤,其发病隐匿,多数患者确诊时已属中晚期,失去了手术治疗的机会。得益于近来不断涌现的新治疗手段,包括精准放疗、介入治疗、靶向治疗以及免疫治疗等,临床医生已经能从每个患者的具体情况入手,结合现有的各种治疗方式,采用个体化综合治疗方案,从而延长患者的生存时间,改善其生活质量。即使是一些合并门静脉主干癌栓的晚期患者,现在也能得到有效治疗。2018年6月,37岁的王涛(化名)不幸被诊断为晚期肝癌,他辗转多家医院后来到首都医科大学附属北京世纪坛医院求治。肝胆肿瘤外科主任彭吉润教授仔细分析患者病情后,联合介入科、肿瘤内科、放疗科等多学科专家为其制定了个体化的综合治疗方案。经过两次开腹手术、两次介入治疗、一个疗程放疗,并结合靶向药物及免疫治疗,如今距确诊肝癌晚期已一年多了,王涛依然积极乐观地生活着,继续与肿瘤做着不懈斗争。因母婴传播,王涛一出生就携带有乙肝病毒,且从未规律进行过抗病毒治疗,肝脏一天天在被病毒侵蚀、破坏着,直到引起了细胞恶变,长了肿瘤,他却浑然不知。去年6月底,他因间断右上腹疼痛半月,在外院诊断为肝癌晚期,前来首都医科大学附属北京世纪坛医院就诊,检查结果显示右肝巨大肿瘤,合并门静脉主干以及左、右分支癌栓,并已出现了黄疸症状。在教科书中,这样的病例已属于手术禁忌症了,预期生存期不会超过三个月。肝胆肿瘤外科彭吉润教授团队经过细致评估,考虑到患者右肝肿瘤体积巨大,剩余肝脏体积不足,无法一次性彻底切除肿瘤,故决定先做第一次手术,取出了门静脉主干及左侧分支内的癌栓,同时把门静脉右支整体结扎,期望肝脏左叶能代偿性增生到足够的体积。术后经过积极对症支持治疗,结合患者个体情况,彭教授团队联合介入科岳振东主任医师又先后两次为患者做了肝右动脉栓塞术。2018年10月患者再次入院,经过前一阶段的个体化综合治疗,影像学显示病人的右肝巨大肿瘤已明显萎缩,左肝也代偿性显著增加。经过精准评估,彭吉润教授认为患者此时已具备了手术切除肿瘤的条件,他抓住时机为患者设计了手术方案。在第二次手术中,他们完整切除了病人的右半肝,取出了门静脉内的复发癌栓,并对左半肝的几个转移病灶进行了微波消融,术后配合局部放疗、靶向治疗及免疫治疗等综合措施,患者恢复良好。多一种治疗,多一种选择;多一分思考,多一分希望。从患者具体病情出发,多学科专家联手,从各自的专业角度提出最适合患者的治疗策略,从而最大程度地改善患者生活质量,延长患者的生存期,北京世纪坛医院的专家们为王涛这样的晚期肝癌患者带来了生的希望。
彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)1638人已读 - 精选 结直肠癌肝转移并非不治之症
彭吉润首都医科大学附属北京世纪坛医院首都医科大学肿瘤医学院北京大学第九临床医学院结直肠癌是我国常见的恶性肿瘤,其发病率居恶性肿瘤发病率第4位,肝脏是结直肠癌最易发生转移的部位。结直肠癌肝转移可分为同时性肝转移和异时性肝转移:部分患者在发现结直肠癌的同时,就已经发生了肝转移,或者是在结直肠癌原发灶根治性切除术后6个月内发生了肝转移,这两种情况都被定义为同时性肝转移癌,这部分病例约占所有结直肠癌患者总数的15-25%;另外,还有大约15-40%的患者,在结直肠癌根治术6个月后发生了肝转移,这种情况被称为异时性肝转移癌。肝转移在结直肠癌患者中是一种非常常见的情况,早年文献报道,若不采取积极治疗,这类患者的中位生存期仅8个月,5年生存率几乎为0。传统上,由于按照肿瘤的分期标准,结直肠癌合并肝转移属于TNM IV期,被认为是晚期肿瘤,因此无论是外科医生,还是病人及其家属,都认为是不治之症。近年来,经过临床实践、探索,人们逐渐认识到,有一部分患者(10-20%)的结直肠癌肝转移病灶是可以通过手术进行根治性切除的,五年生存率可以达到23-58%。结直肠癌肝转移登记网站(www.livermetsurvey.org)2015年的统计资料更是表明,肝脏转移灶无法根治性手术切除的患者,其5年和10年生存率仅分别为9%和4%,而肝脏转移灶能得到根治性手术切除的患者,其5年和10年生存率分别可以达到42%和25%。目前,外科学界针对结直肠癌肝转移患者,已达成了以下共识:经过术前评估,对于在切除结直肠原发病灶同时可切除肝转移病灶的患者,应选择以外科手术(结直肠癌切除+肝转移病灶切除)为核心的综合治疗方案。而对于肝转移灶不能同时行根治性切除的患者,则应选择化疗±靶向治疗为主的挽救性或转化性治疗方案;在此期间,每2个月对这部分患者实施1次可切除性评估,其中一部分患者的转移病灶对药物反应良好,可获得二期手术切除的机会,另一部分患者可继续施行挽救性-转化性治疗,直至能满足二期手术切除的条件。对于异时性肝转移癌患者,选择治疗方案时,亦按照以上共识的原则进行判断。究竟哪些肝转移患者适合外科手术治疗呢?目前认为,只要同时满足以下三个条件,即可考虑手术治疗:(1)肝脏转移病灶可以全部切除或毁损,(2)术后能够保留足够的残余肝脏体积,(3)没有明显的手术禁忌证。对于肝脏转移病灶,除了手术切除外,也可采取微波消融或射频消融进行毁损治疗,或者联合采用手术切除加热消融的方式进行治疗。遇到病灶数目较多,或者转移灶位置特殊、毗邻大血管等重要结构,导致手术切除困难时,采用热消融治疗更具优势:对于前者,消融毁损治疗能保留更多的残肝体积,减少术后发生肝功能衰竭的风险;对于后者,消融治疗可降低治疗病灶的技术难度,更适合肝切除经验较少的单位。具体到技术细节,肝脏转移灶数目的多寡,并非影响手术决策的绝对因素。特别是对肝脏转移灶较多,散布左、右半肝的病例,是否适合外科治疗,除了要考虑病人的年龄、体质、原发病灶情况等常规因素外,往往取决于主治医生的技术和经验。笔者所在团队自2012年起,采用手术切除联合微波消融技术,曾治疗一组结直肠癌肝转移灶数目大于5个甚至10个的患者,均取得了较满意的疗效。其中一例肝脏转移灶数目接近20个的患者,术后生存期达到了五年以上。日本有外科医生曾报告可一次性安全切除一百余个肝脏转移病灶。对于结直肠癌合并同时性肝转移患者,笔者所在团队通常采用腹腔镜切除结直肠原发病灶,从而尽可能减少患者的创伤,随后再于右上腹开腹,直视下或在术中B超导引下,对肝脏病灶进行手术切除或消融治疗。一旦确定拟按上述方法进行手术,那么对原发病灶的治疗一定要按照根治性手术而非姑息性手术的原则进行,否则,术后肿瘤极易复发。对于合并多个肝转移癌的患者,我们的经验是,行开腹手术,并在术中对肝脏进行真正零距离的超声扫查,往往能发现更多术前MRI或CT扫描不能发现的微小病灶,这对于彻底消除肝脏病灶至关重要。随着技术的进步以及治疗理念的改变,结直肠癌肝转移的治疗效果已经较以往得到了很大改善,但是,实际工作中,由于内、外科各专科分科过细、相关专业知识的普及仍存在死角等原因,在很多基层医院,甚至在一些大型医院或肿瘤专科医院,有相当一部分患者也没有得到最为适当的治疗。具体表现在:一些患者只切除了原发病灶,而且往往是按照传统的观念,仅做了原发病灶的姑息性切除,却未处理肝脏转移灶;有些患者的肝转移病灶虽然超过了一个,属于“多发”,但数目较少,完全可以同期或二期手术切除或消融,且技术难度不大,却被推荐到内科进行化疗或靶向药物治疗,当肿瘤的病理类型恰好对这些治疗不敏感时,往往失去了外科治疗的机会;此外,还有一些患者,接受化疗或靶向治疗后,虽然病灶对治疗反应良好,但未及时推荐到外科进行二期手术治疗……凡此种种,都对结直肠癌肝转移的整体疗效产生了极大的负面影响。因此,亟需在医疗专业人员以及患者群体中,进一步普及相关专家共识和治疗理念。小结:(1)结直肠癌合并肝转移,即使是多发肝转移,并非全部都是“晚期”肿瘤,有相当一部分病例仍值得积极地进行以外科手术为主的综合治疗,外科治疗对这些患者而言,仍然起着其它疗法不可替代的决定性作用。(2)对于肝转移灶能够全部切除或消融的患者,应该对其结直肠原发病灶行根治性切除术,而非姑息性手术。(3)相对于术前MRI和CT检查,术中在肝脏表面进行B超扫查可以发现更多的肝转移灶,更有助于达到根治性治疗效果。总之,结直肠癌肝转移并非不治之症,只要选对了正确的诊断和治疗路径,在有经验的医院接受治疗,并配合适当的化疗和各种新兴的免疫疗法,相信有相当一大批结直肠癌肝转移患者会明显获益。(版权所有,转载请注明出处)
彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)5016人已读 - 精选 我校彭吉润教授团队与北大等研究团队联合在Cell发文 首次在单细胞水平描绘肝癌微环境免疫图谱
2017-06-26 17:24 来源:首都医科大学 6月16日,我校彭吉润教授研究团队与北京大学生命科学学院BIOPIC中心、北京未来基因诊断高精尖创新中心、北大-清华生命科学联合中心张泽民研究团
彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)1361人已读 - 精选 我科学家首次详尽揭示肝癌免疫图谱 对研发抗癌新药意义重大
2017-06-26 03:45 来源:光明网-《光明日报》 光明日报记者 詹媛 近日,我国科学家对取自多个肝癌患者的5000余个T细胞逐个进行了基因测序,从而勾勒出每个细胞的基因表达图谱,这是世界上首次对癌症患者体内的T细胞在单细胞层面上进行如此大规模的详尽分析,为未来发现肝癌及其他癌症的免疫疗法奠定了基础。 这项由北京大学生命科学学院BIOPIC中心、北大-清华生命科学联合中心教授张泽民,首都医科大学附属北京世纪坛医院暨北京大学第九临床医学院肝胆胰外科主任彭吉润教授,以及美国安进公司(AMGEN)欧阳文军博士共同合作的研究成果近日发表在国际期刊《细胞》上,本报记者就此独家专访了彭吉润。 发现抗肿瘤药物研制的潜在靶点 “人体内每天都会有无数新细胞诞生,有些可能会在遗传和性能上表现异常,有恶变的倾向,而T细胞作为存在于人体淋巴系统内的免疫细胞,能够监测并攻击这些‘内奸’,将它们及时杀灭。”彭吉润说,尽管如此,肿瘤细胞却能够想尽办法逃过监测,这种现象被称为免疫逃逸,是肿瘤细胞能够躲避攻击、不断增殖的原因。因此,弄清楚肿瘤细胞躲避攻击的原理,就有可能开发出药物“激活”T细胞,让它们杀死肿瘤细胞。 彭吉润介绍,T细胞的功能紊乱和抑制性T细胞的大量存在,是肿瘤细胞逃避人体免疫监测的重要原因,而针对这两类细胞寻找治疗靶点则是免疫疗法的主要方向。“通过某种作用,肿瘤细胞可能会使T细胞过早‘衰老’,或者丧失攻击的‘子弹’,甚至可能被‘策反’,对其他同类也进行抑制。”彭吉润说,此次研究发现肝癌组织内存在大量过早“衰老”的杀伤性T细胞,而在这种类型的T细胞中又发现了抑制型T细胞,据此可以推断出,正常T细胞会先变得“衰老”,继而具有抑制其他同类的功能,这就描绘了肿瘤细胞躲避人体免疫的具体过程。 在此次的研究中,还发现一个被称为Layilin的基因在“衰老”的杀伤性T细胞和抑制性T细胞中都有异常表达,体外实验也证明该基因表达异常对T细胞有抑制调节作用,因此“Layilin基因有可能成为一个免疫疗法的新靶点”。彭吉润表示,这意味着通过对肿瘤细胞与这个靶点间作用机制的研究,未来也许能够开发出对这个靶点起作用的抗癌新药物。 为治疗肝癌提供新可能 “20余年前,人们发现T细胞上存在着程序性死亡受体-1(PD-1)这个靶点,如今对该靶点作用的抗癌药物已经挽救了很多肿瘤患者的生命。”彭吉润说,“PD-1就像是T细胞上的‘刹车器’,肿瘤细胞能拉‘刹车器’,使T细胞‘刹车’,不再攻击肿瘤细胞。” 依据该原理开发的抗癌药物在恶性黑色素瘤和肺癌的治疗上已有显著成果。“这种药物相当于在PD-1上覆盖了一层保护装置,使肿瘤细胞无法拉‘刹车器’,T细胞就会正常攻击。”彭吉润说。然而由于受到DNA变异数目、肿瘤内部存活淋巴细胞的水平以及药物靶点的表达等因素影响,这种药物在不同病人及不同癌症上的效果却很不均一。例如,对大部分肝癌患者、1/3左右的肺癌患者没有明显作用。这就需要进一步详尽研究单细胞水平,发现人体内的淋巴细胞与肿瘤细胞的更多相互作用,为开发新抗癌药探索更多路径。 他介绍,此次发表在《细胞》上的研究成果,对肝癌患者的血液、肿瘤周围、肿瘤与正常组织的交界处以及肿瘤内部提取的5000余个T细胞进行了单细胞分析。“这是一种新兴的生命科学分析方法,通过分析每个细胞的DNA、RNA以及其上诸多分子团的性能,来发现治疗肿瘤的靶点,此次是分析了T细胞上与肿瘤免疫有关的分子团以及其他生物有效标志物,为研制新药做最基础的生命科学层次的探索。”彭吉润说。 “除了Layilin基因,此次所形成的数据库里还蕴藏着很多靶点信息,因此这是一个名副其实的‘宝库’。”彭吉润表示,更多靶点的发现,意味着有可能开发出新型抗癌药物,挽救更多人的生命。 为全球科学家提供数据“宝库” 尽管单细胞分析非常有效,但由于每个细胞上蕴含的遗传和生物信息量特别大,因此需要花费大量的时间和精力,这也是国际上此前从未有过对肿瘤患者体内的免疫细胞进行如此大规模详尽研究的原因之一。而此次的研究整整耗费了3年时间,在国际上首次利用单细胞分析法对如此大量的免疫细胞进行分析,并首次揭示肝癌的详尽免疫图谱,构建了肝癌患者人体免疫细胞基因表达的海量数据库。 对于这项研究,《细胞》期刊一位匿名评审专家在评审意见中迫不及待地表示:“必须要让它尽快发表,因为这些数据实在太有价值了。” “假如把与肝癌相关的免疫细胞的信息比喻成厚厚的一本书,那么我们目前所面对的就是这本书所撕成的碎片,每一个碎片都蕴含着信息,而这次研究所获得的信息量就像这些碎片的数量一样多,是无法计量的海量数据库。”在彭吉润看来,这个数据库中蕴藏着解析人类抗击癌症的大量“密码”,需要科学家们一步步去拼接、解码。 目前,该数据库已向全球开放,有兴趣的科研同行都可获取这些信息。“也许就会有人从中发现对治疗肿瘤有用的信息,从而开发出新的抗肿瘤药物。”彭吉润说,“我们为大家打开了‘宝库’的大门,并拿出了一两件夺目的宝物,而里面究竟还有些什么宝藏,还要继续‘发掘’和‘清点’。” 《光明日报》( 2017年06月26日06版)
彭吉润 主任医师 世纪坛医院 肝胆肿瘤外科(普外科一病区)947人已读





